Estados de Agregación y propiedades de los Gases
Estados de agregación de la materia
La materia se presenta en diferentes estados físicos según la forma en que están organizadas y se mueven sus partículas.
- Sólido
- Forma y volumen definidos.
- Partículas muy juntas, con poca libertad de movimiento (vibran en su sitio).
- Ejemplo: hielo, madera, hierro.
- Líquido
- Volumen definido pero no tienen forma propia, adoptan la del recipiente.
- Partículas más separadas, con capacidad de deslizarse unas sobre otras.
- Ejemplo: agua, aceite, alcohol.
- Gas
- Ni forma ni volumen definidos.
- Las partículas están muy separadas y en movimiento rápido.
- Ejemplo: aire, dióxido de carbono.
- Plasma
- Gas a temperaturas muy altas donde los electrones se separan de los átomos.
- Conduce electricidad y está presente en el Sol, estrellas y lámparas fluorescentes.
Cambios de estado
- Fusión: sólido → líquido.
- Solidificación: líquido → sólido.
- Vaporización: líquido → gas (evaporación o ebullición).
- Condensación: gas → líquido.
- Sublimación: sólido → gas (ejemplo: hielo seco).
- Sublimación inversa: gas → sólido.
Propiedades de los gases
Los gases se diferencian de sólidos y líquidos porque:
- Son compresibles y expansibles.
- Se difunden fácilmente en otro gas.
- Sus partículas se mueven a gran velocidad en todas direcciones.
Leyes de los gases más importantes:
- Ley de Boyle: A temperatura constante, la presión y el volumen son inversamente proporcionales.
$$P⋅V=constante$$
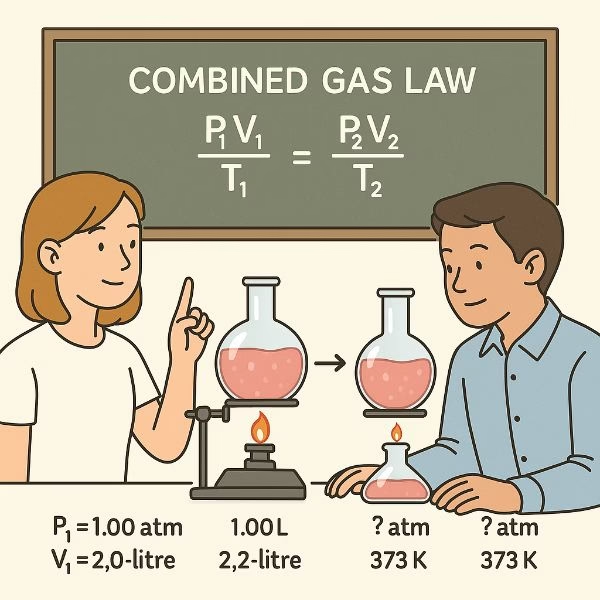
- Ley de Charles: A presión constante, el volumen de un gas aumenta proporcionalmente a la temperatura.
$$V/T=constante$$
- Ley de Gay-Lussac: A volumen constante, la presión de un gas es proporcional a la temperatura.
$$P/T=constante$$
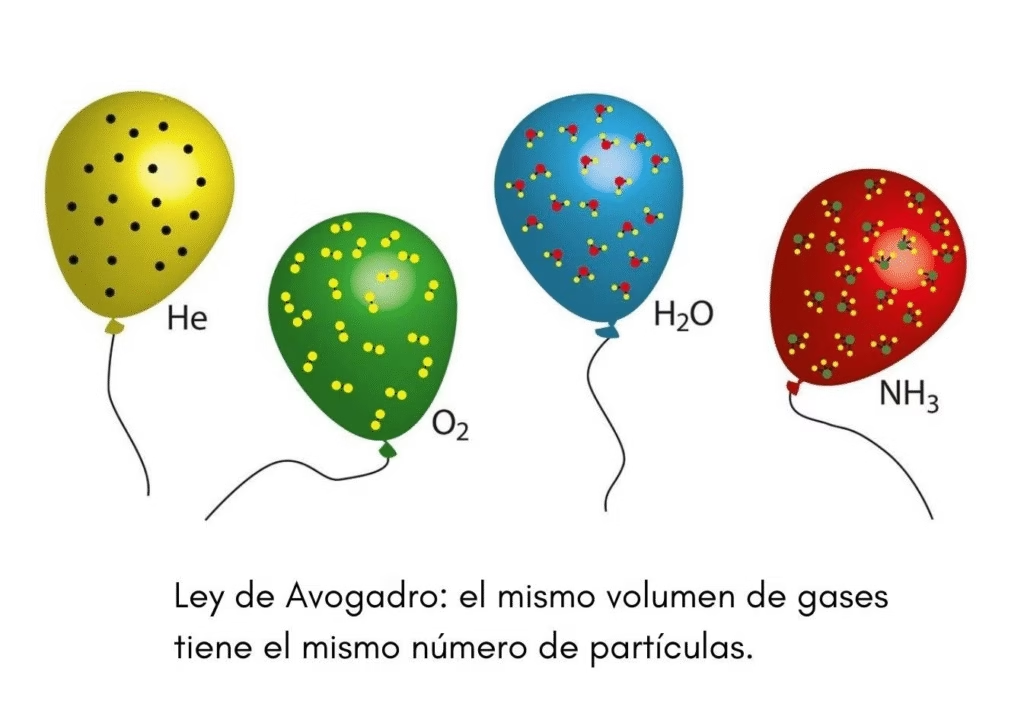
- Ley de Avogadro: Volúmenes iguales de gases, a la misma temperatura y presión, contienen el mismo número de partículas.
Actividad grupal
1. Pensar
Investiga y copia sobre estas propiedades de los gases y copia su fórmula, enfatizando como afectan la difusión, la compresión, la expansión, la presión. Incluye un ejemplo cotidiano de cada una y un dibujo (p. ej., aerosol, jeringa, globo al frío/calor).
- Ley de Boyle
- Ley de Charles
- Ley de Gay-Lussac
- Ley de Avogadro
2. Redactar
Elige un fenómeno real y descríbelo en 6–8 líneas usando las ideas del video:
- ¿Por qué un perfume se huele a distancia?
- ¿Por qué una jeringa funciona?
- ¿Qué le pasa a un balón en la nevera vs. al sol?
3. Crear
Diseña un miniafiche digital que ilustre una de las propiedades y una regla de seguridad para manipular gases.